









Sprawdź odpowiedzi
Poziom 1
A
A–4 B–3 C–2 D–1 E–6 F–5
B
Wiązania chemiczne to trwałe połączenie dwóch atomów przy udziale elektronów walencyjnych znajdujących się na powłokach walencyjnych.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest wiązanie chemiczne
– wskazanie jaka powłoka elektronowa bierze udział z elektronami walencyjnymi
Poziom 2
A
1.F 2.F 3.F 4.P 5.P 6.F 7.P 8.P 9.P 10.P 11.P 12.P 13.F
B
A) H2 – 2 atomy (1 cząsteczka)
B) 2H – 2 atomy
C) 2H2 – 4 atomy (2 cząsteczka)
Wyjaśnienie:
A) Zapis H2 oznacza jedną cząsteczkę wodoru, która składa się z dwóch atomów wodoru połączonych ze sobą wiązaniem kowalencyjnym niespolaryzowanym
B) Zapis 2H oznacza dwa oddzielne atomy wodoru. Nie jest to cząsteczka, a dwa osobne atomy, które nie są ze sobą połączone.
C) Zapis 2H2 oznacza dwie (dwuatomowe) cząsteczki wodoru. Każda z cząsteczek H2 zawiera 2 atomy wodoru
Poprawna odpowiedź powinna zawierać:
– wskazanie ile atomów pokazuje każdy zapis
– wyjaśnienie czym różni się zapis A) B) C)
C
Katalizator to substancja, która zwiększa szybkość reakcji, jednak sama nie ulega trwałym przemianom chemicznym i nie wpływa na jej kierunek.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest katalizator
– wskazanie jak katalizator wpływa na reakcje chemiczne
Poziom 3
A
1) cząsteczka bromu Br2 – wiązanie kowalencyjne niespolaryzowane
2) amoniak – wiązanie kowalencyjne spolaryzowane
3) chlorek sodu – wiązanie jonowe
4) tlenek wapnia – wiązanie jonowe
5) chlorowodór – wiązanie kowalencyjne spolaryzowane
6) cząsteczka tlenu O2 – wiązanie kowalencyjne niespolaryzowane
B
Elektroujemność to zdolność atomu danego pierwiastka do przyciągania elektronów tworzących wiązania chemiczne w danej cząsteczce.
Elektroujemność wzrasta w układzie okresowym pierwiastków chemicznych wraz ze wzrostem numeru grupy i maleje wraz ze wzrostem numeru okresu.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest elektroujemności
– wyjaśnienie zależności elektroujemności w obrębie układu okresowego
C

Poziom 4
A
Wartościowość to maksymalna liczba wiązań tworzonych przez atomy danego pierwiastka.
Pierwiastki z 1 grupy zawsze mają wartościowość: I
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest wartościowość
– wskazanie jaka jest wartościowość pierwiastków z grupy 1
B
Polaryzacja wiązania to zjawisko przesunięcia wspólnej pary elektronowej, tworzącej wiązanie chemiczne w stronę jądra atomu o wyższej wartości elektroujemności.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest polaryzacja wiązania
C
1. woda:
liczba par elektronowych: 2
liczba wolnych par elektronowych: 2
2. siarkowodór:
liczba par elektronowych: 2
liczba wolnych par elektronowych: 2
3. cząsteczka jodu:
liczba par elektronowych: 1
liczba wolnych par elektronowych: 6
D
1. BeO – tlenek berylu
2. Al2O3 – tlenek glinu
3. Cl2O7 – tlenek chloru (VII)
Poziom 5
A

B
Kwas ortokrzemowy (IV) H4SiO4 składa się z atomów wodoru, krzemu i tlenu.
mH = 1u
mSi = 28u
mO = 16u
mH4SiO4 = 4 ∙ 1u + 1 ∙28u+4∙16u= 96u
Odp. Masa cząsteczkowa kwasu ortokrzemowego (IV) wynosi 96u
C
1. kation sodu ma taką samą konfigurację elektronową, jak: Neon
2. anion siarczkowy ma taką samą konfigurację elektronową, jak: Argon
3. kation wapniowy ma taką samą konfigurację elektronową, jak: Argon
4. anion fluorkowy ma taką samą konfigurację elektronową, jak: Neon
5. kation glinu ma taką samą konfigurację elektronową, jak: Neon
Poziom 6
A
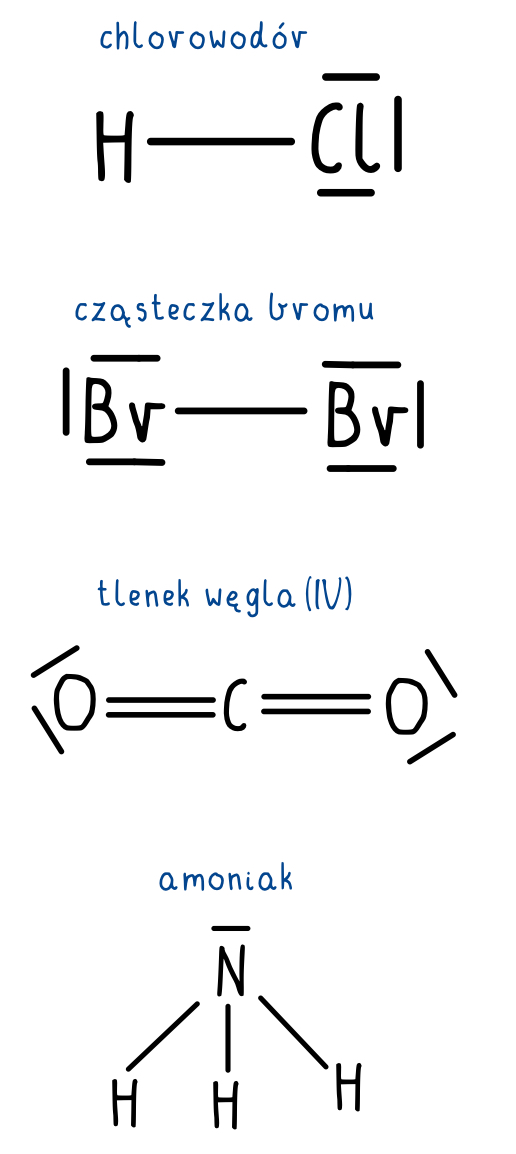
B
1. kation magnezu
Konfiguracja elektronowa: K2L8
2. anion tlenkowy
Konfiguracja elektronowa: K2L8
3. kation wapnia
Konfiguracja elektronowa: K2L8M8
4. kation bromkowy
Konfiguracja elektronowa: K2L8M18N8
Poziom 7
A
mC = 12u
mH = 1u
mCxH10 = 58u
58u – 10u = 48u
48u : 12u = 4
x = 4
Odp. Indeks stechiometryczny x wynosi 4 – C4H10
B
1. 2Mg + O2 –> 2MgO
Substraty: magnez, tlen
Produkty: tlenek magnezu
Typ reakcji chemicznej: synteza (łączenia)
2. 2H2+ O2 –> 2H2O
Substraty: wodór, tlen
Produkty: woda
Typ reakcji chemicznej: synteza (łączenia)
2. 2HgO –> 2Hg + O2
Substraty: tlenek rtęci (II)
Produkty: rtęć, tlen
Typ reakcji chemicznej: analizy (rozkładu)
C
mO = 12g
mHg = mO + 64g = 12g + 64g = 76g
mHgO = mHg + mO = 12g + 76g = 88g
Odp. Tlenek rtęci (II) przed termicznym rozkładem ważył 88g.
Poziom 8
A
Reakcjami chemicznymi rządzą dwa prawa: Prawo zachowania masy i Prawo stałości składu. Jedno z nich głosi, że masa substratów musi być równa masie produktów. Prawo to nazywa się: Prawo zachowania masy. Stosunek masowy pierwiastków w związku chemicznym jest wielkością stałą i charakterystyczną dla związku. Prawo stałości składu informuje nas, że stosunek masowy pierwiastków w związku chemicznym jest wielkością stałą.
Chemik upiekł wczoraj ciasto owocowe. Użył 300 g mąki, 2 jajka, 20 g cukru i 200g owoców. Ciasto urosło, jak by było na drożdżach. Ciasto ważyło około 530 gramów. Chemik zaobserwował działanie prawa zachowania masy, ponieważ np. masa substratów jest równa masie produktów – ciasto powinno ważyć tyle samo ile substancje które wchodzą w jego skład.
Poprawna odpowiedź powinna zawierać:
– uzupełnienie luk w tekście
– wyjaśnienie podanej obserwacji
B
Typ reakcji: wymiany
Suma współczynników stechiometrycznych: 5
C
Wiązanie wodorowe – oddziaływanie występujące pomiędzy atomem wodoru, a atomem o wysokiej elektroujemności (najczęściej fluor, azot, tlen).
Np.

Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest wiązanie wodorowe
– pokazanie mechanizmu powstawania wiązania wodorowego