






Sprawdź odpowiedzi
Poziom 1
A
1.N 2.R 3.R 4.N 5.R 6.N 7.N 8.T
R – rozpuszczalne
T – trudnorozpuszczalne
N – nierozpuszczalne
B
1.P 2.F 3.F 4.P 5.F 6.F 7.P 8.P 9.F 10.P 11.P 12.P 13.P
Poziom 2
A
1. chlorek litu – LiCl
2. chlorek glinu – AlCl3
3. siarczek żelaza (III) – Fe2S3
4. siarczek miedzi (II) – CuS
5. bromek wapnia – CaBr2
6. bromek cynku – ZnBr2
7. azotan (V) baru – Ba(NO3)2
8. azotan (V) manganu (IV) – Mn(NO3)4
9. azotan (V) glinu – AlPO4
10. fosforan (V) srebra (II) – Ag3(PO4)2
11. siarczan (IV) miedzi (II) – CuSO3
12. azotan (VI) berylu – BeSO4
B
1. KCl – chlorek potasu
2. CaCl2 – chlorek wapnia
3. Cu2S – siarczek miedzi (II)
4. FeS – siarczek żelaza (II)
5. AlBr3 – bromek glinu
6. MgBr2 – bromek magnezu
7. Sr(NO3)2 – azotan (V) strontu
8. AgNO3 – azotan (V) srebra (I)
9. FePO4 – fosforan (V) żelaza (III)
10. Be3(PO4)2 – fosforan (V) berylu
11. CuSO3 – siarczan (IV) miedzi (II)
12. Li2SO4 – siarczan (VI) litu
Poziom 3
A
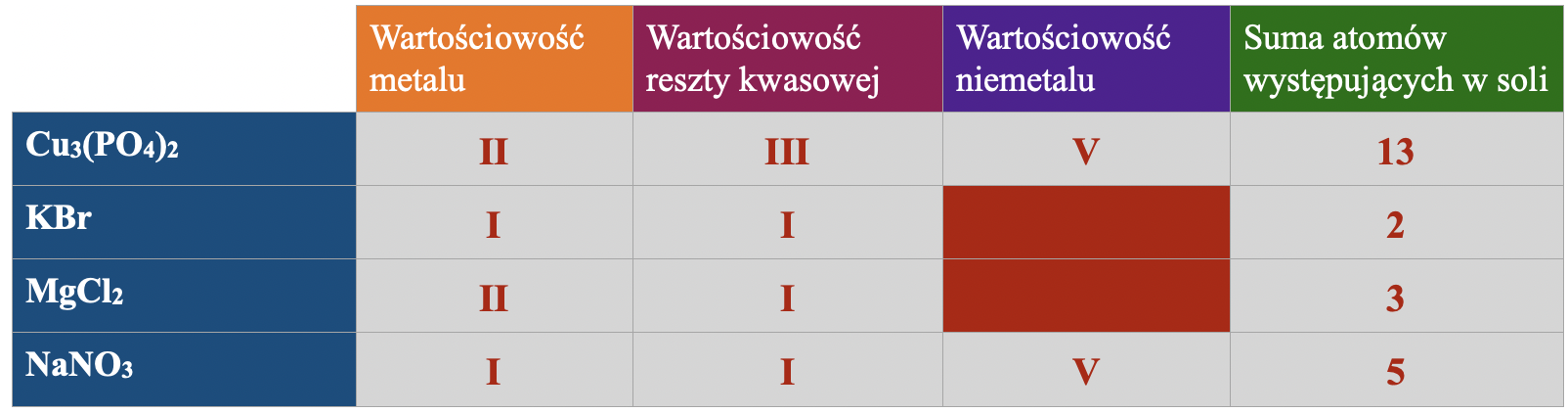
B
Reakcja zobojętnienia to reakcja pomiędzy kwasem, a wodorotlenkiem (zasadą) z utworzeniem soli. Ubocznym produktem jest woda.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest reakcja zobojętnienia
– wskazanie czym są substraty i produkty reakcji neutralizacji
Poziom 4
A
1. składnik soli drogowej – chlorek sodu, chlorek potasu
2. składnik nawozów sztucznych – azotan (V) sodu, azotan (V) potasu, fosforan (V) sodu
3. składnik proszku do pieczenia – wodorowęglan sodu
4. Produkcja szkła, środek antypoślizgowy dla wspinacza – węglan magnezu (magnezyt)
5. m.in jako kreda tablicowa – węglan wapnia (kalcyt)
Podano przykładowe wzory sumaryczne soli, które są nawozami oraz zastosowanie soli 4. 5.
Poziom 5
A
3. Al2(SO4)3 —> 2Al3+ + 3SO42- [pod wpływem wody]
5. Zn(NO3)2 —> Zn2+ + 2NO3– [pod wpływem wody]
B
1. wodorotlenek potasu + kwas fosforowy (V)
OH– + H+ —> H2O
2. wodorotlenek wapnia + kwas azotowy (V)
OH– + H+ —> H2O
3. wodorotlenek sodu + kwas siarkowy (VI)
OH– + H+ —> H2O
Poziom 6
A
2. Uzupełnione równanie reakcji chemicznej: 2K + H2SO4 –> K2SO4 + H2
B
2. Uzupełnione równanie reakcji chemicznej: 2Na + 2HCl –> 2NaCl + H2
Poziom 7
A
Forma jonowa skrócona: Ca2+ + 2OH– —> Ca(OH)2
B
Poziom 8
A
2. W której probówce, powstaje osad ? Probówka A
3. Opisz obserwację w probówce D: Roztwór się odbarwił z malinowej barwy.
– podanie obserwacji wynikającej z równania reakcji w probówce D
– NIE WSKAZANIE WZÓRÓW SUMARYCZNYCH / NAZW SYSTEMATYCZNYCH ZWIĄZKÓW CHEMICZNYCH
B
– wskazanie zlewki A w której wytraca się osad
– podanie argumentu, dlaczego w zlewce A wytrąca się osad
C
Napisz nazwy systematyczne dla podanych soli:
1. (NH4)3PO4 – fosforan (V) amonu
2. Mg(MnO4)2 – manganian (VII) magnezu
3. Cr(NO3)6 – azotan (V) chromu
4. NaHCO3 – wodorowęglan sodu