






Sprawdź odpowiedzi
Poziom 1
A
Woda jest najbardziej znanym na świecie związkiem chemicznym i najbardziej rozpowszechnionym. Jest go aż 73% na kuli ziemskiej. Woda może być słodka i słona. 70% to woda słona, a tylko 3% to woda słodka, którą pijemy i jest zawarta m.in w lodowcach. Dzięki właściwościami fizycznymi woda tworzy obieg zamknięty. Woda wrze w temperaturze 100°C, krzepnie w 0°C, a największą gęstość w temperaturze 4°C.
B
Poziom 2
A
Napięcie powierzchniowe to rodzaj oddziaływania, w którym powierzchnia wody zachowuje się jak sprężysta błona, podczas kontaktu z ciałem stałym, cieczą lub gazem.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest napięcie powierzchniowe
– określenie zjawiska tego jako „sprężysta błona”
B
Poziom 3
A
1.F 2.P 3.P 4.P 5.F 6.P 7.P 8.P 9.F 10.P
B
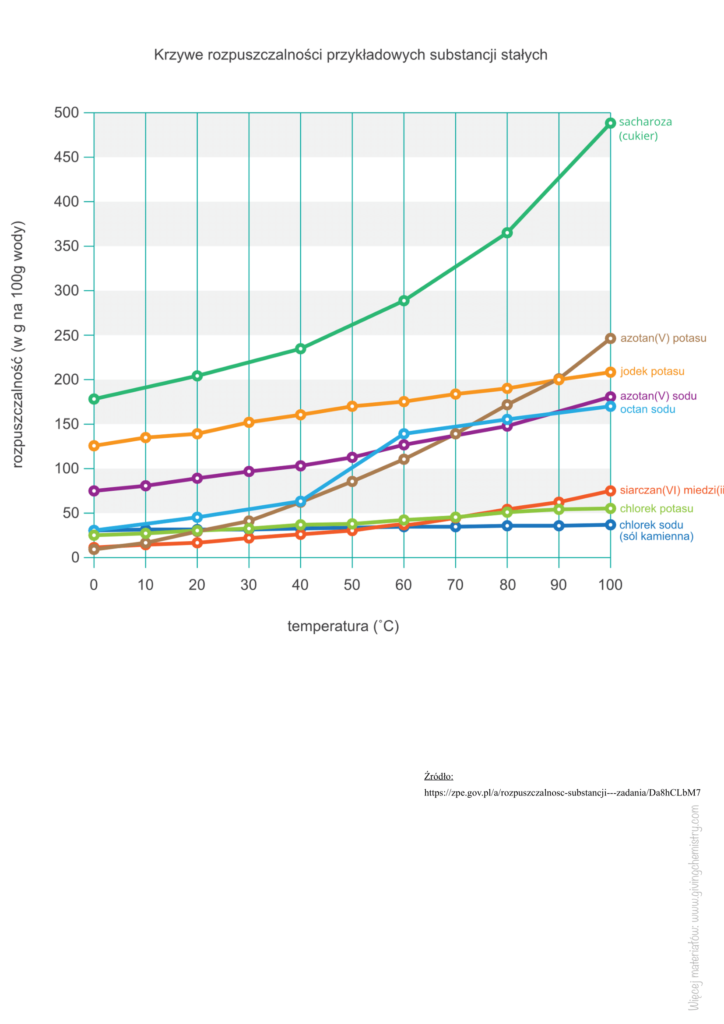
Rozpuszczalność to maksymalna liczba gramów substancji, którą można rozpuścić w 100 g rozpuszczalnika w danej temperaturze (i pod danym ciśnieniem). W efekcie powstaje roztwór nasycony.
Rozpuszczanie to proces fizyczny, ponieważ nie powstają nowe substancje o odmiennych właściwościach chemicznych / drobiny mieszają się z drobinami rozpuszczalnika.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest rozpuszczalność
– określenie czy rozpuszczanie to proces fizyczny, czy reakcja chemiczna
Poziom 4
A
B
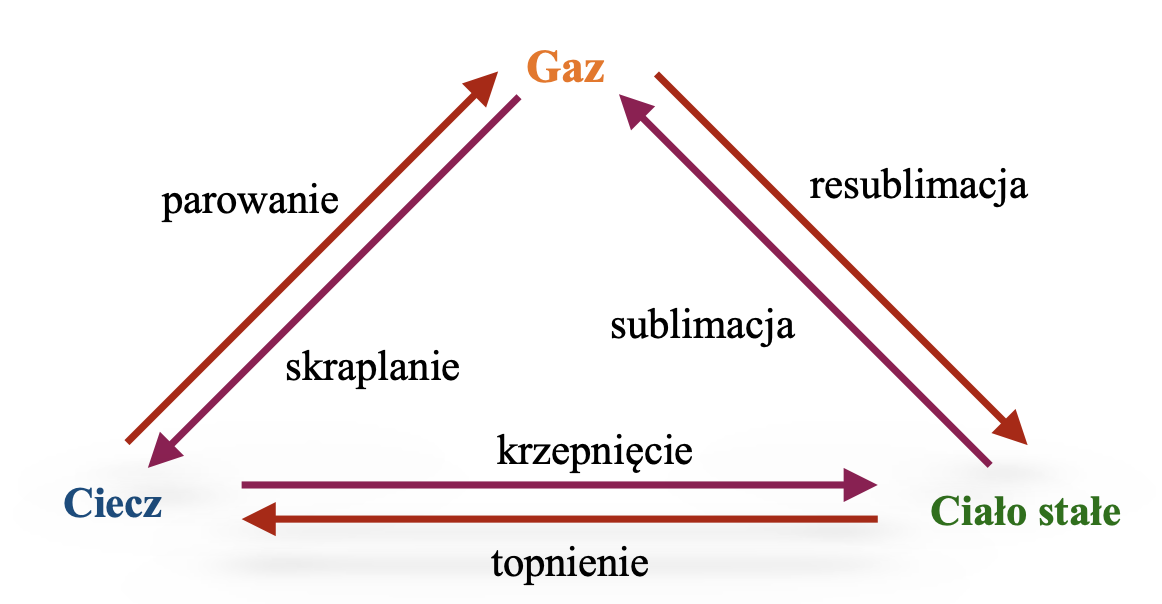
1. Metoda: dodanie wody / ogrzanie roztworu
2. Metoda: odparowanie wody / oziębienie roztworu / dodanie substancji
3. Metoda: oziębienie roztworu
4. Metoda: dodanie wody / ogrzanie roztworu
5. Metoda: dodanie rozpuszczalnika / usunięcie części substancji rozpuszczonej
Poziom 5
A
Dane:
mH2O = 300 g
Z wykresu odczytujemy, że na 100 g wody można rozpuścić 140 g octanu sodu w temperaturze 60°C, aby otrzymać r-r nasycony.
Szukane:
mr =?
Metoda:
Układamy proporcję, aby obliczyć masę substancji rozpuszczonej:
100 g wody – 140 g octanu sodu (wynika z analizy wykresu)
300 g wody – x g octanu sodu (z polecenia)
x = 420 g (taką ilość octanu sodu możemy rozpuścić w 300 g wody, aby otrzymać r-r nasycony).
Korzystając z definicji masy roztworu, obliczamy masę roztworu:
mr = ms + mrozp.
mr = 420 g + 300 g = 720 g
Odp. Masa nasyconego roztworu wynosi 720 g
! Masa roztworu może różnić się nie znacząco, w wyniku innej przyjętej wartości rozpuszczalności soli na wykresie !
B
Dane:
mH2O = 440 g
Z wykresu odczytujemy, że na 100 g wody można rozpuścić 160 g jodku potasu w temperaturze 40°C, aby otrzymać r-r nasycony.
Szukane:
mr =?
Cp =?
Metoda:
Układamy proporcję, aby obliczyć masę substancji rozpuszczonej:
100 g wody – 160 g jodku potasu (wynika z analizy wykresu)
440 g wody – x g jodku potasu sodu (z polecenia)
x = 704 g (taką ilość jodku potasu możemy rozpuścić w 440 g wody, aby otrzymać r-r nasycony).
Korzystając z definicji masy roztworu, obliczamy masę roztworu:
mr = ms + mrozp.
mr = 704 g + 440 g = 1144 g
Korzystając ze wzoru na stężenie procentowe, obliczamy Cp:
Cp = (ms : mr ) ∙ 100%
Cp = (704 : 1144) ∙ 100%
Cp ≈ 52,2%
Odp. Stężenie procentowe nasyconego roztworu w temperaturze 40°C wynosi ok. 61,5%
! Stężenie procentowe może różnić się nie znacząco, w wyniku innej przyjętej wartości rozpuszczalności soli na wykresie !
Poziom 6
A
Woda to przykład związku chemicznego o budowie polarnej. Substancja polarna posiada dwa różne bieguny elektryczne + i –.
W cząsteczce wody występują wiązania kowalencyjnie spolaryzowane. Jest dipolem, ponieważ biegun ujemny znajduje się bliżej tlenu, a biegun dodatni obok wodoru.
Budowa polarna umożliwia rozpuszczanie się substancji (związków chemicznych) w wodzie.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest budowa polarna
– określenie budowy dipola
– podanie cechy budowa, która ułatwia rozpuszczanie się substancji w wodzie
B
Zawiesina – rodzaj mieszaniny niejednorodnej, w których cząsteczki rozmiar większy niż 500 nm. Jesteśmy w stanie odróżnić poszczególne składniki – substancje mieszaniny.
Np.
– woda z piaskiem
– kawa z fusami
– sok pomarańczowy z miąższem
Koloid – rodzaj mieszaniny niejednorodnej, w których cząsteczki rozmiar od 1 nm do 500 nm. Nie jesteśmy w stanie odróżnić poszczególne składniki – substancje mieszaniny.
Np.
– mleko
– masło
– żelatyna
Roztwór właściwy – rodzaj mieszaniny jednorodnej, w których cząsteczki rozmiar mniejszy niż 1 nm. Nie jesteśmy w stanie odróżnić poszczególne składniki – substancje mieszaniny.
Np.
– woda z solą/cukrem
– woda z alkoholem etylenowym
– sok jabłkowy
Poprawna odpowiedź powinna zawierać:
– podanie definicji podanych roztworów
– określenie czy dany roztwór należy do mieszaniny jednorodnych / mieszaniny niejednorodnych
Poziom 7
A
Dane:
Cp1 = 24 %
ms = 120 g
Szukane:
mH2O =?
Metoda:
Korzystając ze wzoru obliczamy masę roztworu:
Cp = (ms : mr ) ∙ 100%
Cp∙ mr = ms ∙ 100%
mr = (ms ∙ 100%) : Cp
mr = (120 ∙ 100%) : 24% = 500 g
Korzystając z definicji masy roztworu, obliczamy masę rozpuszczalnika:
mr = ms + mrozp.
mrozp. = mr + ms
mrozp. = 500 g + 120 g = 380 g
Odp. Oby przyrządzić 24% r-r chlorku sodu należy rozpuścić 120 g soli w 380 g wody.
B
Z zadania wynika, że do roztworu 1 o określonym stężeniu dodano dodatkową porcję substancji rozpuszczonej. W efekcie powstał roztwór 2 – bardziej stężony/
Dane:
Cp1 = 8 %
mr = 320 g
m =88 g
Szukane:
ms1 =?
ms2 =?
mr2 =?
Cp2 =?
Metoda:
Korzystając ze wzoru obliczamy masę substancji w roztworze 1:
Cp1 = (ms1 : mr1 ) ∙ 100%
Cp1∙ mr1 = ms1 ∙ 100%
ms1 = (Cp1 ∙ m1r) : 100%
ms1 = (8% ∙ 320 g) : 100% = 25,6 g
! Masa substancji nie ubywa !
Obliczamy masę substancji po dodaniu dodatkowej porcji:
ms2 = ms1 + m
ms2 = 25,6 g + 88 g = 113,6 g
Obliczamy masę roztworu po dodaniu dodatkowej porcji:
mr2 = mr1 + m
mr2 = 320 g + 88 g = 408 g
Obliczamy stężenie roztworu 2, do który powstał w wyniku dodania 88 g sacharozy do roztworu 1:
Cp = (ms : mr ) ∙ 100%
ms = (113,6 : 408 ) ∙ 100% ≈ 27,8 %
Odp. Stężenie procentowe roztworu sacharozy po dodaniu 88 g cukru do roztworu 1 (o Cp = 8%) wynosi ok.27,8%
! Stężenie procentowe może różnić się nie znacząco, w wyniku innego zaokrąglenia masy substancji 1 !
Poziom 8
A
Efekt Tyndalla to zjawisko fizyczne, polegające na rozpraszaniu światła przez koloid z wytworzeniem charakterystycznego stożka świetlnego.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym jest Efekt Tyndalla
– wskazanie efektu zjawiska – charakterystyczny stożek
B
Dane:
mH2O = 300 g
– Z wykresu odczytujemy, że na 100 g wody można rozpuścić 140 g octanu sodu w temperaturze 60°C, aby otrzymać r-r nasycony.
– Z wykresu odczytujemy, że na 100 g wody można rozpuścić 60 g octanu sodu w temperaturze 40°C, aby otrzymać r-r nasycony.
Szukane:
mr = ?
Metoda:
Układamy proporcję, aby obliczyć masę substancji rozpuszczonej w temp.60°C:
100 g wody – 140 g octanu sodu (wynika z analizy wykresu)
300 g wody – x g octanu sodu (z polecenia)
x = 420 g (taką ilość octanu sodu możemy rozpuścić w 300 g wody, aby otrzymać r-r nasycony).
Układamy proporcję, aby obliczyć teoretyczną masę substancji rozpuszczonej w temp.400°C:
100 g wody – 60 g octanu sodu (wynika z analizy wykresu)
300 g wody – x g octanu sodu (z polecenia)
x = 180 g (taką ilość octanu sodu możemy teoretycznie rozpuścić w 300 g wody, aby otrzymać r-r nasycony).
Obliczamy masę soli, która wykrystalizuje w niższej temperaturze (60°C do 40°C):
ms-wykrystalizowana = ms-60°C + ms-400°C
ms-wykrystalizowana = 420 g – 180 = 240 g
Odp. Podczas oziębienia roztworu octanu sodu z temp.60°C do 40°C wykrystalizuje się 240 g soli.