






Sprawdź odpowiedzi
Poziom 1
A
N – azot
tlen – O
Br – brom
krzem – Si
C – węgiel
wapń – Ca
Fe – żelazo
glin – Al
Na – sód
chlor – Cl
Cu – miedź
złoto – Au
B
Przykładowa odpowiedź:
Ciała stałe mają określony kształt oraz objętość, ich cząsteczki znajdują się blisko siebie. Ich cząsteczki nie mogą się swobodnie przemieszczać.
Ciecze mają określoną objętość, natomiast przyjmują kształt naczynia, w którym się znajdują. Ich cząsteczki znajdują się blisko siebie, ale nie są tak ciasno upakowane, jak w ciałach stałych. Mogą się one swobodnie przemieszczać, co pozwala na cieczy na płynięcie.
Gazy nie posiadają określonego kształtu i objętości. Przyjmują one kształt i wypełniają objętość w dostępnej przestrzeni. Ich cząsteczki są znacznie oddalone od siebie, poruszają się swobodnie we wszystkich kierunkach, często się zderzając o siebie i ze ścianami naczynia.
Poprawna odpowiedź powinna zawierać:
– opis właściwości substancji w stanie stałym
– opis właściwości substancji w stanie ciekłym
– opis właściwości substancji w stanie gazowym
Poziom 2
A
1. elektrony znajdują się na 5 powłokach elektronowych: wszystkie pierwiastki z 5 okresu (np. rubid, stront, srebro, pallad, kadm, cyna, jod, ksenon)
2. posiada 0 elektronów: wodór (prot)
3. potas jest aktywniejszy niż: sód (oraz inne pierwiastki, które są od niego aktywniejsze)
B
grupa 1 – LitowceC
Zastosowania izotopów m.in: medycyna leczenie i rozpoznawanie chorób), archeologia (określanie wieku minerałów), źródło energii, w przemyśle i technice (biotechnologia).
Poziom 3
A
1.P 2.F 3.P 4.F 5.P 6.P 7.F 8.F 9.F 10.F 11. P 12.F 13.P
B
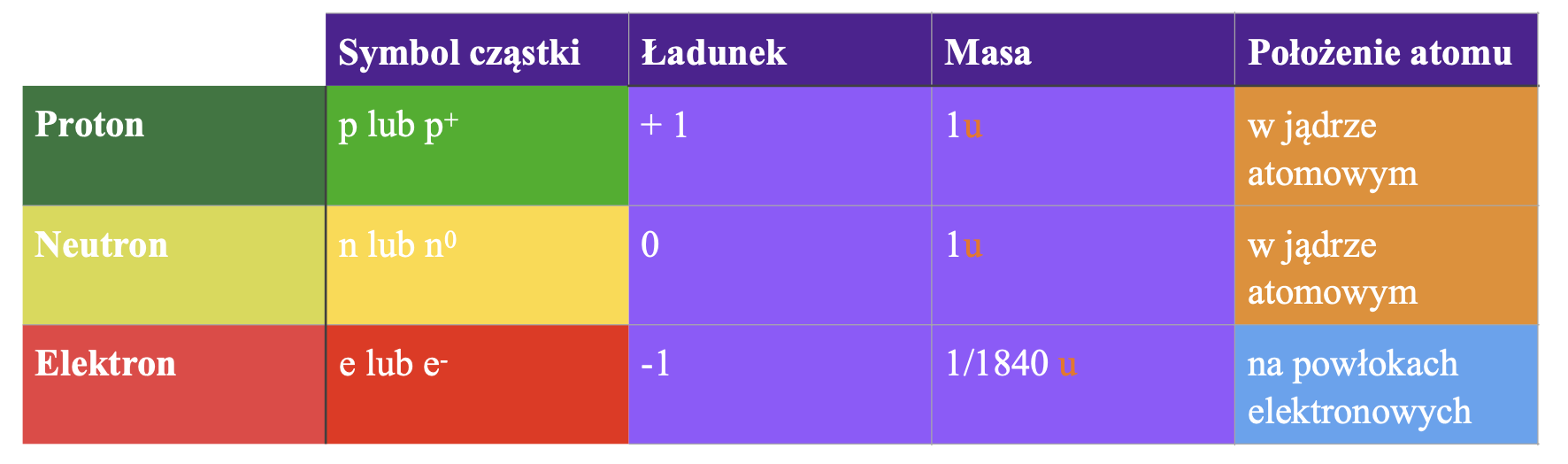
Poziom 4
A
A1
P – fosfor
p+ = 15
e– = 15
e– walencyjne = 5
n0 = 16
nukleony = 31
B2
Se – selen
p+ = 34
e– = 34
e– walencyjne = 6
n0 = 45
nukleony = 79
B
więcej / 12 u / Lit / mało / 18
C
Symbol: Cl (chlor)
Poziom 5
A
Przykładowy rysunek modelu atomu dla atomu wapnia:

Zapis konfiguracji elektronowej: K2L8M8N2
Przykładowy rysunek modelu atomu dla atomu fosforu:

Zapis konfiguracji elektronowej: K2L8M5
B
Wzór na średnią masę atomową:
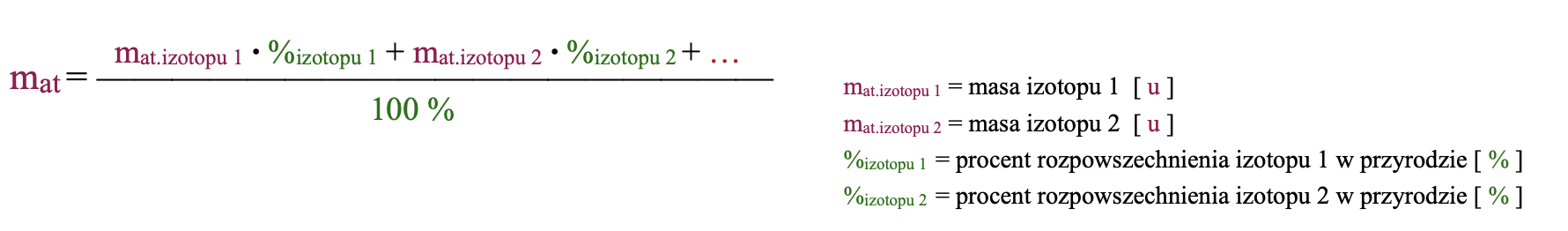
Na potrzeby zapisu zamienimy procenty na liczby.
mat = (34,97 • 0,758) + (36,97 • 0,242) = 26,51 + 8,95 = 35,46
Średnia masa atomowa chloru wynosi: 35,46
Poziom 6
A
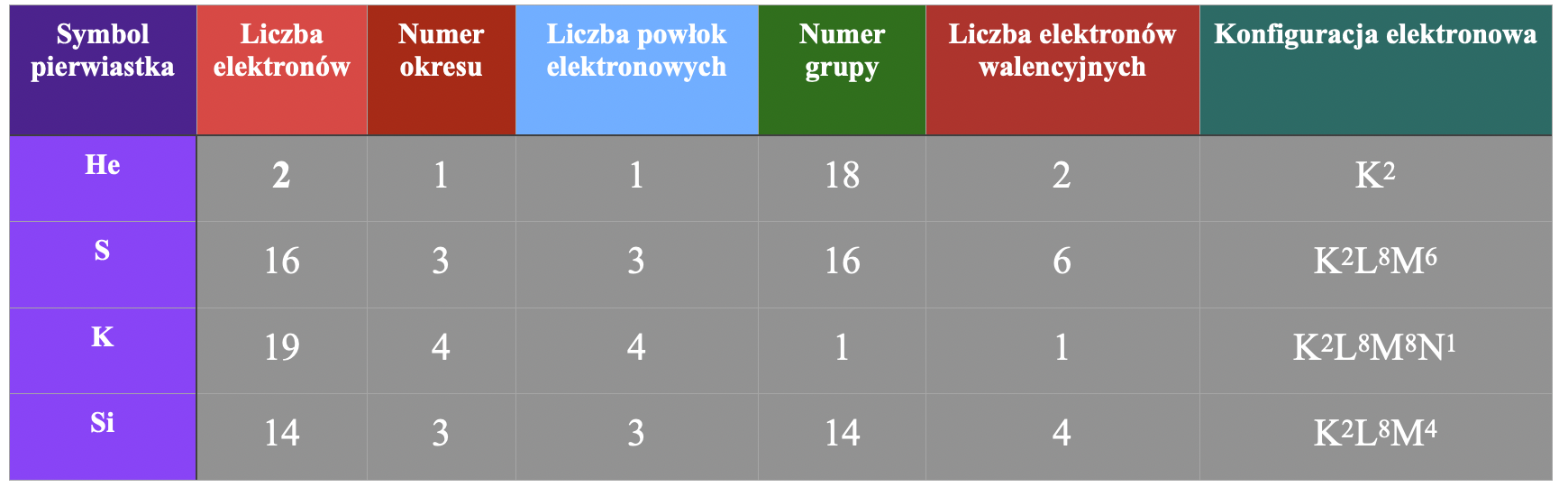
B
Przykładowa odpowiedź:
Dyfuzja zjawisko samorzutnego mieszania się substancji w wyniku chaotycznego poruszania się ich drobin. Dyfuzja zachodzi najszybciej w gazach, a najwolniej w ciałach stałych.
Np. Drobiny perfum mieszają się w powietrzu – mieszanina jednorodna
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie, procesu dyfuzji
– podanie 1 przykładu zjawiska dyfuzji
Poziom 7
A
Przykładowa odpowiedź:
Izotopy to atomy tego samego pierwiastka, które różnią się liczbą neutronów w jądrze atomowym, czyli liczbą masową „A„
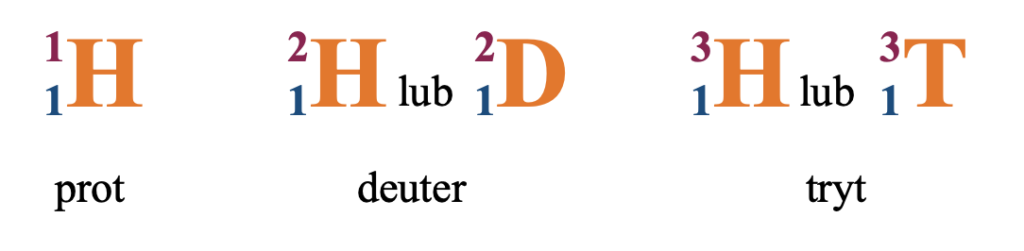
Prot:
p+ = 1
e– = 1
n0 = 0
Deuter:
p+ = 1
e– = 1
n0 = 0
Tryt:
p+ = 1
e– = 1
n0 = 0
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie czym są izotopy
– wymienienie 3 naturalnych izotopów wodoru – prot, deuter i tryt.
– zapis liczby protonów, elektronów i neutronów dla każdego izotopu
Poziom 8
A
Przykładowa odpowiedź:
A) Liczba powłok elektronowych w atomie pierwiastka chemicznego odpowiada numerowi okresu, w którym on leży.
B) Liczba e– walencyjnych odpowiada numerowi grupy głównej (1-2 i 13-18). Przykładowo tlen (O) znajduje się w 16 grupie i posiada 6 elektronów walencyjnych.
C) Aktywność metali rośnie w dół grupy i w lewo w okresie, co znaczy, że najaktywniejsze metale znajdują się w lewym dolnym rogu układu okresowego.
Jeśli chodzi o niemetale, to ich aktywność rośnie w górę grupy i w prawo w okresie, co znaczy, że najaktywniejsze niemetale znajdują się w prawym górnym rogu układu okresowego (z wyłączeniem grupy 18 – gazów szlachetnych).
D) Metale posiadają tendencję do oddawania elektronów, tworząc przez to kationy. Zdolność do oddawania elektronów wzrasta w dół grupy.
Niemetale jednak mają tendencję do przyjmowania elektronów, tworząc w ten sposób aniony. Zdolność do przyjmowania elektronów wzrasta w górę grupy i w prawo w okresie.
E) Liczba atomowa pierwiastków rośnie z lewej do prawej w okresach i z góry na dół w grupach. Wzrost liczby atomowej oznacza więcej protonów (p+) i elektronów (e–), co wpływa na właściwości chemiczne oraz fizyczne pierwiastków.
Do tego kryterium, wybierzmy sód (Na). Leży on w grupie 1, okresie – 3. Jego liczba atomowa wynosi 11, l. powłok – 3. Sód posiada 1 e– walencyjny. Metal ten jest miękki i srebrzysty. Jest bardzo reaktywny (szczególnie z wodą).W reakcjach chemicznych łatwo oddaje jeden elektron – tworząc kation Na+.
Aktywniejszym od niego pierwiastkiem może być np. lit (Li). Również znajduje się on w 1 grupie, a to, ze jest bardziej aktywny od sodu, spowodowane jest tym, że e– walencyjne w licie są bliżej jądra atomowego i silniej przyciągane, co czyni go bardziej skłonnym do oddawania elektronu w reakcjach chemicznych.
Poprawna odpowiedź powinna zawierać:
– wyjaśnienie podpunktów A, B, C, D, E
– podanie i wyjaśnienie pierwiastka, który jest aktywniejszy od badanego pierwiastka